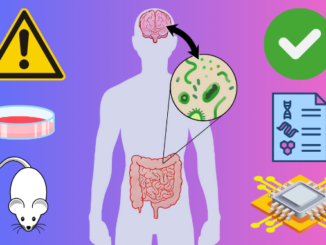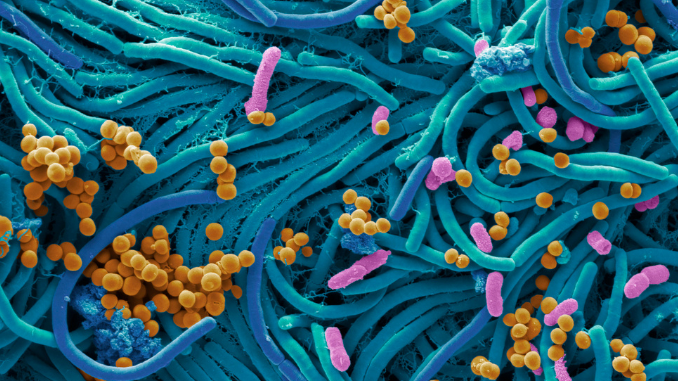
Sappiamo oggi che la flora microbica intestinale gioca un ruolo chiave per l’organismo e che uno suo squilibrio è in grado di determinare alterazioni su numerose funzioni organiche; non solo, sappiamo anche che lo stato di salute influisce sulla composizione ed eventuale squilibrio del microbiota.
In questo studio si è concentrata l’attenzione sugli organ on-chip di intestino, che meglio ricapitolano la barriera aerobica e anaerobica presente a livello intestinale. Nel lume intestinale la concentrazione di ossigeno molto scarsa o assente, favorisce lo sviluppo di microrganismi anaerobi, ma nel contempo in prossimità delle cellule epiteliali intestinali che necessitano di ossigeno, la tensione del medesimo è tale da consentire anche lo sviluppo di una flora aerobica. La riproposizione delle diverse modulazioni gassose risulta dunque di fondamentale importanza per capire gli sviluppi del microbiota e le relative interazioni farmacologiche utili allo sviluppo di terapie orali. Sono molteplici le condizioni che modificano il microbiota intestinale e nel contempo le alterazioni del microbiota sono in grado di influenzare il sistema immunitario e lo stato di salute.
A livello intestinale, la presenza di muco è fondamentale per separare la popolazione batterica luminale dalle cellule epiteliali e altrettanto importante il gradiente di ossigeno che si viene a determinare lungo il villo. Il muco dell’area contigua al villo è al contempo una sede di sviluppo e nutrimento per i batteri non strettamente anaerobi, che consumando l’ossigeno a disposizione ne determinano l’aumento del gradiente di concentrazione.
I modelli animali messi a punto per gli studi sul microbiota, si sono rivelati più spesso non rappresentativi dal punto di vista fisiologico, sono mancanti di predittività, costosi ed eticamente discutibili. I metodi alternativi si possono avvalere sia di test in silico, ma soprattutto di test in vitro che partendo dalle cellule Caco2 di adenocarcinoma colon-rettale, si sono poi evoluti ai tessuti derivanti dalle cellule iPSC (staminali pluripotenti indotte), fino ad arrivare ad organoidi e organi on chip. In particolare è con lo sviluppo dei sistemi microfluidici che si è avuta una svolta decisiva. Quest’ultimi infatti hanno permesso di ricreare membrane porose permeabili ai fluidi ma anche ai gas, favorendo la riproposizione in sito dei diversi gradienti di ossigeno; non solo, un altro aspetto saliente riguarda la motilità meccanica e la stimolazione cellulare da parte del flusso fluidico che è in grado di esercitare quelle forze e pressioni che in vivo regolano la riproduzione batterica e favoriscono lo sviluppo dei villi. Il flusso crea uno stress da taglio alle cellule epiteliali che sono indotte a proliferare, mentre esercita una down-regulation sulla crescita batterica. Il sistema microfluidico è in grado inoltre di modulare la concentrazione di ossigeno. Gli studi sull’intestino on-chip hanno rivelato come i batteri commensali migliorano l’attività della barriera intestinale, mentre viceversa i patogeni ne diminuiscono le potenzialità di barriera. Pertanto il sistema è ottimale anche per discriminare la flora commensale da quella patogena. Gli attuali paradigmi di ricerca sempre più evoluti, ci conducono non tanto verso un unico modello di intestino su chip, quanto piuttosto su modelli diversi e specifici per le diverse esigenze di ricerca che si presentano di volta in volta. Gli elementi su cui puntare l’attenzione per migliorare le prestazioni di queste metodologie sono la capacità di controllo del gradiente di ossigeno e la possibilità di misurarlo; ma ancora un ruolo chiave lo svolgono i materiali impiegati nella fabbricazione, che dovranno presentare le giuste caratteristiche in fatto di permeabilità all’ossigeno e di idrofilicità. Possibilmente questi materiali dovrebbero assomigliare alla matrice extracellulare intestinale sia in fatto di caratteristiche meccaniche, sia biochimiche (es.proteine presenti in vivo). Dovrebbe essere implementato il ruolo della barriera tra epitelio ed endotelio che non sempre è accuratamente rappresentata ed ha invece un ruolo chiave. Per quanto riguarda la peristalsi meccanica si è visto che favorisce la proliferazione e la differenziazione delle cellule Caco-2, ma necessita di ulteriore approfondimento. Da sottolineare l’importanza decisiva per questo tipo di ricerche, sia della rilevazione degli effetti meccanici di proliferazione/contenimento legate allo stress da taglio, sia dello studio della barriera e delle sue alterazioni di permeabilità in particolare tramite una metodica non invasiva come il TEER (resistenza elettrica transepiteliale/transendoteliale). Nel prossimo futuro bisognerà poi prevedere l’implementazione di questi modelli sulla base dell’asse cervello/intestino, sembra infatti che le interconnessioni siano piuttosto significative. Per quanto concerne poi il microbiota sappiamo che esso varia in ragione del tratto intestinale di appartenenza, dell’individuo e addirittura presenta fluttuazioni giornaliere; tutto questo per dire che non è facile riproporre su chip le diverse interazioni microbiche presenti in vivo, ma si sta lavorando anche a questo. Un altro elemento da non banalizzare è la conoscenza dei tempi di rinnovamento cellulare nei diversi compartimenti intestinali. Da ultimo, ma fondamentale al pari di tutto quanto è già stato raccomandato, vi è la standardizzazione dei modelli, il libero accesso a documenti e ricerche per evitare inutili perdite di tempo e la definizione di protocolli di ricerca validi per tutti i laboratori.
Elsbeth G.B.M.Bossink, Loes I.Segerink, MathieuOdijk. Organ-on-Chip Technology for Aerobic Intestinal Host – Anaerobic Microbiota Research. Sciencedirect Volume 4, December 2022, 100013. https://doi.org/10.1016/j.ooc.2021.100013