Cos’è la sperimentazione animale?
“Sperimentazione Animale” (s.a.) è un termine ombrello che racchiude tutte queIIe tecniche di ricerca, non necessariamente cruente, che fanno uso di animali vivi. Dagli esperimenti che comportano operazioni chirurgiche e quindi il taglio dei tessuti, ai test di tossicità acuta e cronica, agli studi che prevedono l’induzione di malattie, lesioni e traumi fino alla morte.
Riportiamo solo alcuni esempi recenti di studi su animali finalizzati alla ricerca medica, approvati dagli Organismi Preposti al Benessere Animale o equivalenti, conformi quindi alle normative europee o statunitensi in materia di “benessere animale”. Sebbene la sperimentazione animale in Europa ed USA sia regolamentata, il grado di stress e dolore che essa comporta agli animali può essere molto elevato.
Modello animale di danno da denervazione parziale per lo studio del dolore orofacciale
Si pratica incisione della regione infraorbitaria del ratto (sotto anestesia) e dopo che l’animale ha recuperato dall’effetto dell’anestetico la zona dissezionata chirurgicamente viene esposta ad iniezioni di formalina onde indurre il dolore orofacciale.
Studio del dolore reumatico nei roditori
I classici modelli di dolore infiammatorio acuto includono l’iniezione nella zampa posteriore dei roditori di sostanze chimiche (ad esempio, formalina o carragenina), che producono una rapida risposta nocicettiva caratterizzata da leccamento e scuotimento della zampa (formalina), e diminuite soglie di risposta agli stimoli termici o meccanici (cioè, allodinia e iperalgesia). Il dolore neuropatico negli animali è classicamente modellato da interventi che causano un certo grado di danno ai nervi, come legatura o costrizione cronica.
Modello murino di peritonite settica
Induzione di peritonite nel topo attraverso inserimento chirurgico di uno stent a livello del colon ascendente allo scopo di studiare la sepsi.
Entro poche ore dall’intervento, gli animali mostrano i primi segni clinici di sepsi: mobilità ridotta, deterioramento del pelo, sudorazione, riduzione dell’assunzione di cibo, perdita di peso e riduzione del comportamento di fuga. Gli animali che sviluppano una peritonite grave con infezione sistemica normalmente muoiono entro 48 ore. A seconda della dimensione dello stent inserito, è possibile generare tassi di mortalità distinti, dal 100 al 50%.
Modello murino di infarto miocardico
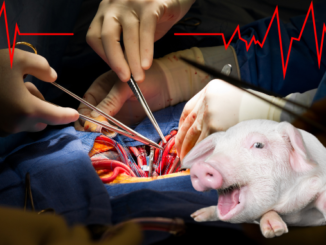
Induzione di ischemia miocardica nel topo mediante legamento chirurgico di un’ arteria coronaria. Lo scopo è quello di simulare l’infarto e la conseguente disfunzione cardiaca nei pazienti umani.
Modello di trombosi carotidea (cane)
Modello di trombosi carotidea nel cane. In questo studio viene adattato al cane il protocollo comunemente usato nei piccoli animali.
Modello murino di depressione post-partum
Esposizioni delle femmine di ratto in allattamento a stress ripetuto generato dalla presenza di un intruso. Misurazione di parametri biochimici e comportamentali per lo studio della depressione post partum.
Carini, L. M., Murgatroyd, C. A., Nephew, B. C. Using Chronic Social Stress to Model Postpartum Depression in Lactating Rodents. J. Vis. Exp. (76), e50324, doi:10.3791/50324 (2013).
Misurazione dei comportamenti correlati a prurito e dolore nei topi
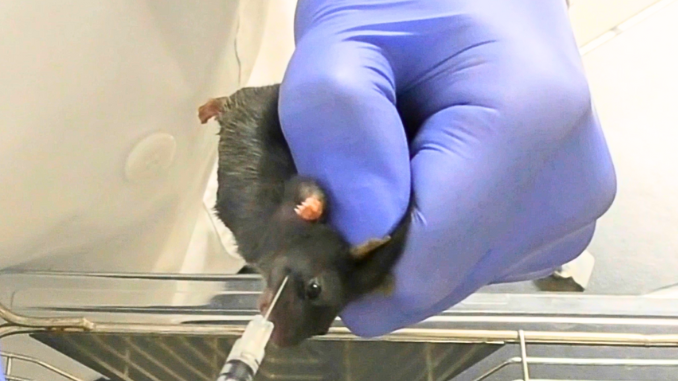
Esperimenti che prevedono l’iniezione di sostanze fortemente algogene (che provocano dolore) nella guancia del topo, per osservarne gli effetti sul comportamento. Questo tipo di esperimenti non prevede anestesia e necessita di immobilizzare gli animali durante le iniezioni, per evitare che i movimenti dovuti all’ iniezione dolorosa inficino la riuscita dell’esperimento.
Modelli murini di trauma
- Modello di shock emorragico: un catetere viene inserito nell’arteria femorale del topo e viene prelevato il 35-60% del sangue
- Modello di trauma cranico: craniotomia (apertura del cranio) seguita dal dispiegamento di un impattatore ad azionamento pneumatico che misura 3 mm a una velocità di 5-6 m/sec
- Frattura delle ossa lunghe:
- Femore: l’osso è esposto e fratturato tramite osteotomia (recisione chirurgica) o dopo averlo indebolito con diversi fori. La frattura del femore può essere seguita dal posizionamento di un perno endomidollare (dentro il midollo dell’osso), un chiodo di bloccaggio o una vite di compressione endomidollare.
- Pseudofrattura: lesione da schiacciamento muscolare bilaterale agli arti posteriori con iniezione di una soluzione a base di osso nei muscoli lesionati
- Trauma toracico: ad es. si colpisce il torace laterale con un impattatore, con una velocità di 5,8 m/s e un’energia di 152 J/m2 provocando una contusione polmonare… oppure si ventilano gli animali con volumi correnti di 15-45 mL/kg di peso corporeo (eccessivi) per indurre lesioni polmonari
- Politrauma: ad es. il topo viene posto in un tamburo di metallo e fatto rotolare ripetutamente, producendo modelli di lesioni variabili… oppure si inducono shock emorragico, frattura delle ossa lunghe, lesione dei tessuti molli e laparotomia (apertura della parete addominale attraverso incisione) con rimozione dell’intestino cieco.
Julie A. Stortz, Steven L. Raymond, Juan C. Mira, Lyle L. Moldawer, Alicia M. Mohr, Philip A. Efron, Murine Models of Sepsis and Trauma: Can We Bridge the Gap?, ILAR Journal, Volume 58, Issue 1, 2017, Pages 90–105, https://doi.org/10.1093/ilar/ilx007
Modelli animali di abuso fisico e sessuale
Diversi studi hanno sviluppato modelli animali di abuso fisico e sessuale, spesso infliggendo sofferenze estreme agli animali con il pretesto di studiare gli effetti della violenza sull’uomo. Alcuni esperimenti hanno simulato lesioni cerebrali e strangolamento nei ratti per analizzare l’impatto della violenza domestica, mentre altri hanno riprodotto abusi sessuali infantili immobilizzando coniglietti e inserendo palloncini nell’ano per simulare uno stupro. Altri studi hanno esposto femmine di ratto a maschi aggressivi per osservare le reazioni comportamentali e cognitive, con alcuni esperimenti che hanno forzato interazioni sessuali violente tra ratti. Per approfondire vi invitiamo a leggere questo articolo dove sono reperibili anche le fonti bibliografiche.
Oltre all’inevitabile stress procurato dalle pratiche sperimentali vere e proprie, gli animali risentono anche delle condizioni innaturali di vita negli stabulari e dello stress procurato dalle pratiche routinarie quali manipolazioni, prelievi, misurazioni, ecc.