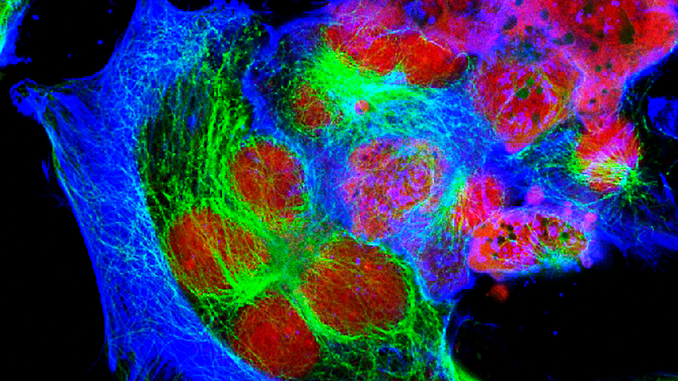
Il Neuroblastoma è un tumore solido extracranico che colpisce soprattutto nella prima infanzia con prognosi ancora troppo spesso infausta. E’ un tumore maligno che trae origine da cellule primitive del sistema nervoso autonomo. Sulla base dell’età del soggetto e della tipologia di alterazione genica in atto, i bambini affetti da neuroblastoma di stadio elevato, nonostante la chemioterapia e la radioterapia hanno una prognosi infausta che supera il 40%. Per migliorare la comprensione dei processi insiti nello sviluppo tumorale, occorre comprendere a fondo le dinamiche di interazione tra le cellule cancerose e quelle sane e le modalità con le quali il tumore realizza la sua espansione (vasi sanguigni, tessuto connettivo). Non solo, è altresì fondamentale comprendere il ruolo dell’espressione genica tenendo presente che questa non solo differisce tra i diversi tipi di tumore, ma anche tra un malato e l’altro. Per questa ragione è più che mai importante lo sviluppo di sistemi tissutali microfluidici derivati da cellule tumorali umane, ma con la presenza di vasi sanguigni e cellule staminali mesenchimali che sono necessarie per la stabilizzazione e propagazione della vascolarizzazione. L’obiettivo è testare i farmaci in modo da trovare quello più efficace per il singolo soggetto, con i minori effetti collaterali possibili. Si è dapprima stampato il supporto del modello, lo si è poi inciso per ricavarne la struttura speculare sulla quale la bio-stampante 3D potesse iniettare idrogel (polimeri dispersi in acqua a costituire un materiale biocompatibile) e componenti cellulari per la produzione della parte vascolare. Per quanto concerne il tessuto tumorale, si è provveduto a formare a partire da cellule tumorali ad alto grado, sferoidi poi collocati tra i vasi sanguigni. La cosa sorprendente che si è potuta osservare è che a partire da 6 giorni dopo la messa in coltura globale, i vasi avevano avvolto gli sferoidi e in alcuni casi erano anche penetrati al loro interno. Sono state notate due diverse modalità di sviluppo degli organoidi:
- una nella quale gli sferoidi sono stati avvolti esternamente dai vasi, cresciuti anche al loro interno, ma nonostante ciò la massa si è poco sviluppata; lo si è paragonato alla forma tumorale incapsulata meno aggressiva;
- una nella quale si è assistito alla migrazione delle cellule tumorali (preventivamente colorate con un marker fluorescente) che hanno utilizzato i vasi per raggiungere il tessuto circostante, mimando un’attività metastatica precoce.
Al momento è ancora oggetto di studio cosa determini un fenotipo tumorale piuttosto di un altro, ma comunque in entrambi i modelli si è riscontrata l’attrazione dei vasi sanguigni, l’angiogenesi tumorale e la metastatizzazione. E’ necessario comprendere se il diverso comportamento sotteso all’espressione dei due fenotipi, sia da ricondursi a fattori meccanici connessi al posizionamento degli sferoidi in fase di allestimento, piuttosto che a fattori intrinseci tumorali o ancora all’ambiente specifico di sviluppo. In quest’ultimo caso sarà importantissimo capire se le cellule staminali mesenchimali derivate da adipociti, in grado di differenziarsi in diversi tipi cellulari, possano avere un ruolo nell’indirizzare la diversa progressione del tumore e se questo possa essere a sua volta correlato a caratteristiche individuali connesse anche all’età e al genere.
Nothdurfter D, Ploner C, Coraça-Huber DC, et al. 3D bioprinted, vascularized neuroblastoma tumor environment in fluidic chip devices for precision medicine drug testing. Biofabrication. 2022;14(3). https://doi.org/10.1088/1758-5090/ac5fb7.