Un articolo pubblicato recentemente sulla rivista scientifica Frontiers Drug Discovery, presenta un argomento convincente per l’eliminazione dell’uso dei topi come passaggio intermedio nei test di tossicità dei farmaci.
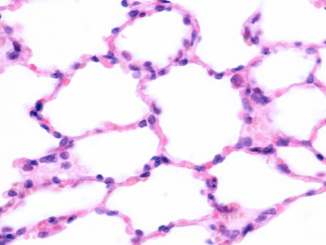
La prognosi per le persone nate con la fibrosi cistica (FC) era un tempo infausta: il sapore salato durante il bacio a un neonato era un segno di una malattia mortale. Le scoperte della ricerca negli anni hanno portato all’identificazione del gene responsabile della malattia e alla creazione di modelli animali per studiare la FC. Tuttavia, Nonostante l’esistenza di oltre 690 modelli murini modificati geneticamente per la CF, gli autori sottolineano che i principali progressi nella ricerca sulla CF spesso derivano da interventi centrati sull’uomo come centri CF, trapianti di polmone e screening neonatale. Tradizionalmente, gli animali sono stati utilizzati nello sviluppo di farmaci per dimostrarne la sicurezza, ma con tassi di abbandono dei farmaci superiori al 90%, è evidente che gli animali non sono sempre predittivi per gli esseri umani. I costi e il tempo necessari per sviluppare modelli animali per l’ampio spettro di mutazioni della FC riscontrate nell’uomo sono esorbitanti, per un totale di oltre 8 milioni di dollari statunitensi per una sola mutazione.
Sfortunatamente, i requisiti normativi attuali ancora prescrivono la sperimentazione di tossicità nei modelli animali, nonostante il loro limitato valore predittivo a causa dell’assenza di coinvolgimento respiratorio nei topi, ad esempio. Tali test- sottolineano gli autori – vengono richiesti anche se i farmaci sono stati sviluppati utilizzando modelli avanzati non animali di ultima generazione.
Gli interventi incentrati sull’uomo hanno svolto un ruolo significativo nel migliorare la comprensione della FC, portando ad un aumento dell’età media di sopravvivenza per i bambini nati con questa condizione. I nuovi approcci metodologici (NAMs) che utilizzano cellule, tessuti e organi umani, dati umani e modelli computerizzati offrono un approccio più rilevante e affidabile per comprendere e trattare le malattie. Questi metodi possono inoltre portare a risparmi sostanziali sui costi di sviluppo dei farmaci.
L’uso di sistemi basati su cellule umane per lo sviluppo di farmaci, come organoidi intestinali e colture di cellule epiteliali delle vie aeree, ha portato a scoperte significative nel trattamento della FC. Questi strumenti consentono lo screening di centinaia di potenziali farmaci e l’identificazione di trattamenti specifici per il paziente, cosa non possibile utilizzando modelli animali. Inoltre, i sistemi basati su cellule umane forniscono informazioni sull’associazione tra fisiologia e sintomi della malattia, consentendo la stima del probabile effetto clinico di un farmaco e i confronti tra diverse mutazioni.
I NAMs focalizzati sulla biologia umana hanno dimostrato successo anche nel riutilizzo dei farmaci, evitando la necessità di test di sicurezza lunghi e costosi necessari per i nuovi composti. L’applicazione di strumenti rilevanti per l’uomo nel riutilizzo dei farmaci ha portato alla scoperta di nuovi trattamenti per varie malattie e condizioni, tra cui COVID-19, neuropatie rare e tossicità renale indotta da farmaci.
Il caso della FC è un esempio significativo di come l’inclusione di strumenti non basati su modelli animali nel processo i sviluppo dei farmaci possa essere rivoluzionario e positivo. I sistemi basati su cellule umane offrono infatti un approccio più rilevante, efficiente e affidabile allo sviluppo di farmaci, portando a scoperte significative nella comprensione e nel trattamento delle malattie. Questo cambiamento di approccio ha il potenziale per accelerare l’accesso a farmaci sicuri ed efficaci per tutti i pazienti.
Gli autori delineano tre raccomandazioni chiave per incoraggiare l’adozione diffusa di metodi non animali nello sviluppo di farmaci, basandosi sul caso di studio della fibrosi cistica:
1. Trasparenza normativa:
- È fondamentale la trasparenza da parte delle agenzie regolatorie, che dovrebbero pubblicare i dati accettati ottenuti con i nuovi approcci metodologici basati sulla biologia umana per evitare inutili sperimentazioni sugli animali. Ciò impedirebbe ai ricercatori di ripetere studi sugli animali quando esistono già alternative efficaci.
2. Potenziamento delle biobanche:
- Incentivare le biobanche, specialmente per malattie rare come la fibrosi cistica, è cruciale. Queste biobanche conservano campioni derivati dai pazienti (cellule, tessuti) permettendo l’accesso globale a ricercatori di tutto il mondo per sviluppare test di valutazione per potenziali farmaci. È importante che il materiale biologico nelle biobanche rispecchi la diversità della popolazione umana.
3. Riorganizzazione dei finanziamenti:
- Le agenzie di finanziamento dovrebbero analizzare i progetti che falliscono e non producono i risultati previsti, in particolare quelli che si basano fortemente su modelli animali. Capire dove i modelli animali falliscono consentirebbe di interrompere i finanziamenti a tali ricerche e allocare risorse verso metodi più promettenti come studi in vitro (su cellule), ricerche epidemiologiche e modelli al computer.
Queste raccomandazioni sono in linea con l’opinione pubblica. Le persone, tramite tasse e donazioni, giocano un ruolo significativo nel sostenere la ricerca e spesso preferiscono alternative alla sperimentazione animale. La Humane Society degli Stati Uniti ha intrapreso azioni in Maryland, introducendo una legge che richiede ai laboratori di ricerca sugli animali di contribuire a un fondo per lo sviluppo di metodi non animali, stabilendo un precedente positivo per il futuro. Se le agenzie governative di finanziamento si impegnassero a spostare il 5-10% dei loro budget verso la ricerca non animale, ciò accelererebbe scoperte scientifiche come i farmaci per la terapia della fibrosi cistica.
Articolo originale per approfondire:
Marshall, L. J., & Conlee, K. M. (2024). The case of the missing mouse—developing cystic fibrosis drugs without using animals. 4. doi:10.3389/fddsv.2024.1347246